Schwefeloxid Formel, Eigenschaften, Risiken und Verwendungen
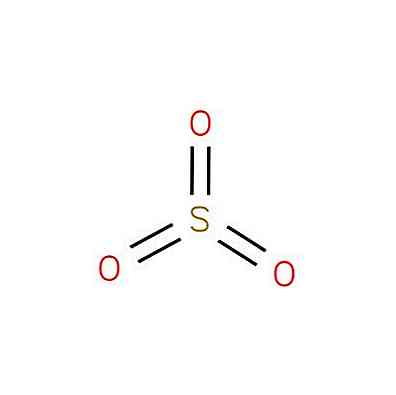
Die Schwefeloxid (VI), auch bekannt als Schwefeltrioxid oder Schwefelsäureanhydrid, ist eine chemische Verbindung der Formel SO3. Seine Struktur ist in Abbildung 1 dargestellt (EMBL-EBI, 2016).
Schwefeltrioxid wird in einer verdünnten gasförmigen Form in einer Kontaktschwefelsäureanlage durch Oxidation von Schwefeldioxid enthaltenden Gasen hergestellt.
Bislang jedoch die einzige Zubereitung von reinem Schwefeltrioxid aus SO-haltigen Gasen3 verdünnt, war es ein Verfahren im Pilotmaßstab, das die kryoskopische Kondensation einschloss.
Das übliche Verfahren beinhaltet stattdessen die Destillation von Oleum. Die für die Oleumdestillation erforderliche Wärme wird am günstigsten durch heißes Kontaktgas aus der zugehörigen Schwefelsäureanlage geliefert.
Es kann im Labor hergestellt werden, indem rauchende Schwefelsäure erhitzt und das Sublimat in einem gekühlten Behälter gesammelt wird. Wenn der Dampf über 27ºC kondensiert, wird die Gamma-Form als eine Flüssigkeit erhalten.
Wenn der Dampf unter 27ºC kondensiert und in Gegenwart einer Feuchtigkeitsspur, wird eine Mischung der drei Formen erhalten. Die 3 Formen können durch fraktionierte Destillation getrennt werden.
Physikalische und chemische Eigenschaften von Schwefeloxid
Schwefeltrioxid ist wie weiße Nadeln geformt, die in der Luft zu Rauch werden. Es trifft häufig auf Hemmstoffe, um die Polymerisation zu verhindern (Nationales Zentrum für Biotechnologie, 2017).
Sein Molekulargewicht beträgt 80,066 g / mol, seine Dichte 1,92 g / cm³ g / ml, und die Schmelzpunkte und Siedepunkte von 16,8 ° C und 44,7 ° C auf. (Royal Society of Chemistry, 2015).
Die Verbindung wird mit Wasser mit explosiver Kraft kombiniert, wobei Schwefelsäure aufgrund ihrer Acidität gebildet wird. Schwefeltrioxid karbonisiert organische Substanzen.
Schwefeltrioxid absorbiert schnell Feuchtigkeit und emittiert dichten weißen Rauch. Die Trioxidlösungen in Schwefelsäure werden rauchende Schwefelsäure oder Oleum genannt. (Schwefeltrioxid, 2016).
Die Reaktion von Schwefeltrioxid und Sauerstoffdifluorid ist sehr stark und Explosionen treten auf, wenn die Reaktion in Abwesenheit eines Lösungsmittels durchgeführt wird. Die Reaktion von überschüssigem Schwefeltrioxid mit Tetrafluorethylen verursacht die explosive Zersetzung von Carbonylfluorid und Schwefeldioxid.
Die Reaktion von wasserfreier Perchlorsäure mit Schwefeltrioxid ist heftig und begleitet von starker Wärmeentwicklung. Schwefeltrioxidflüssigkeit reagiert heftig mit Nitrilchlorid, selbst bei 75 ° C.
Die Reaktion von Schwefeltrioxid und Bleioxid verursacht eine weiße Lumineszenz. Die Kombination von Iod, Pyridin, Schwefeltrioxid und Formamid entwickelte nach mehreren Monaten eine Gasüberdruckbeaufschlagung.
Dies ist aufgrund der langsamen Bildung von Schwefelsäure, Wasser oder wasserentziehenden externer Formamid zu Cyanwasserstoff (Schwefeltrioxids, S.F.).
Reaktivität und Gefahren
Schwefeltrioxid ist eine stabile Verbindung, die mit organischen Materialien, fein gemahlenen Metallen, Basen, Wasser, Cyaniden und einer Vielzahl anderer Chemikalien nicht kompatibel ist.
Die Substanz ist ein starkes Oxidationsmittel und reagiert heftig mit brennbaren und reduzierenden Materialien und organischen Verbindungen, die Brand- und Explosionsgefahr verursachen.
Reagiert heftig mit Wasser und feuchter Luft unter Bildung von Schwefelsäure. Die Lösung in Wasser ist eine starke Säure, sie reagiert heftig mit Basen und sie sind korrosive Metalle, die entflammbares / explosives Gas bilden.
Die Verbindung ist korrosiv gegenüber Metallen und Geweben. Verursacht Verätzungen an Augen und Haut. Verschlucken verursacht schwere Verbrennungen in Mund, Speiseröhre und Magen. Dampf ist sehr giftig beim Einatmen. (Nationales Institut für Arbeitssicherheit und Gesundheit, 2015)
Bei Kontakt mit den Augen sollten Sie überprüfen, ob Sie Kontaktlinsen tragen und diese sofort entfernen. Die Augen sollten mindestens 15 Minuten mit fließendem Wasser gespült werden, wobei die Augenlider offen bleiben müssen. Sie können kaltes Wasser verwenden. Salbe sollte nicht für die Augen verwendet werden.
Wenn die Chemikalie mit Kleidung in Berührung kommt, entfernen Sie sie so schnell wie möglich und schützen Sie Ihre Hände und Ihren Körper. Stellen Sie das Opfer unter eine Sicherheitsdusche.
Wenn sich die Chemikalie auf der freiliegenden Haut des Opfers ansammelt, wie z. B. die Hände, waschen Sie die Haut vorsichtig und vorsichtig mit fließendem Wasser und nicht scheuernden Seifen ab. Sie können kaltes Wasser verwenden. Bei anhaltender Reizung einen Arzt aufsuchen. Kontaminierte Kleidung vor erneutem Tragen waschen.
Bei Einatmen sollte das Opfer in einem gut belüfteten Bereich ruhen. Wenn die Inhalation schwer ist, sollte das Opfer so schnell wie möglich in einen sicheren Bereich evakuiert werden. Lockere Kleidung wie Hemdkragen, Gürtel oder Krawatte.
Wenn das Opfer Schwierigkeiten beim Atmen hat, sollte Sauerstoff verabreicht werden. Wenn das Opfer nicht atmet, wird eine Mund-zu-Mund-Beatmung durchgeführt.Berücksichtigen Sie immer, dass es für die Person, die Hilfe leistet, gefährlich sein kann, eine Mund-zu-Mund-Beatmung durchzuführen, wenn das inhalierte Material toxisch, infektiös oder ätzend ist.
In allen Fällen sollte sofortige medizinische Hilfe in Anspruch genommen werden (Sicherheitsdatenblatt Schwefeltrioxid, 2013).
Verwendet
Schwefeltrioxid ist ein essentielles Reagens in Sulfonierungsreaktionen. Diese Verfahren liefern Detergentien, Farbstoffe und Pharmazeutika. Es wird in situ aus Schwefelsäure erzeugt oder als rauchende Schwefelsäurelösung verwendet.
Die Luftverschmutzung durch Schwefeloxide ist ein großes Umweltproblem, da jährlich Millionen von Tonnen Schwefeldioxid und Trioxid in die Atmosphäre emittiert werden. Diese Verbindungen sind schädlich für das Pflanzen- und Tierleben sowie für viele Baumaterialien.
Ein anderes großes Problem ist saurer Regen. Beide Schwefeloxide lösen sich in atmosphärischen Wassertröpfchen auf, um saure Lösungen zu bilden, die sehr schädlich sein können, wenn sie in Form von Regen verteilt werden.
Es wird vermutet, dass Schwefelsäure die Hauptursache für den Säuregehalt von saurem Regen ist, der Wälder schädigen und in vielen Seen zum Tod führen kann.
Saurer Regen ist auch korrosiv gegenüber Metallen, Kalkstein und anderen Materialien. Mögliche Lösungen für dieses Problem sind teuer aufgrund der Schwierigkeit, Schwefel aus Kohle und Öl zu entfernen, bevor sie verbrennen (Zumdahl, 2014).
Referenzen
- EMBL-EBI (2016, 2. Dezember). Schwefeltrioxid. Von ChEBI abgerufen: ebi.ac.uk
- Sicherheitsdatenblatt Schwefeltrioxid. (2013, 21. Mai). Von sciencebab: sciencebek.com
- Nationales Zentrum für Biotechnologie Information. (2017, 24. Juni). PubChem Compound-Datenbank; CID = 24682 . Von PubChem abgerufen: publem.ncbi.nlm.nih.gov
- Nationales Institut für Arbeitssicherheit und Gesundheit. (2015, 22. Juli). Schwefeltrioxid. Von cdc.gov: cdc.gov abgerufen
- Royal Society of Chemistry. (2015). Schwefeltrioxid. Von chemespider: chemspider.com
- Schwefeltrioxid. (2016). Von chemicalbook: chemicalbook.com.
- Schwefeltrioxid. (S.F.) Von CAMEO: cameochemicals.noa.gov.
- Zumdahl, S. S. (2014, 13. Februar). Von britannica: britannica.com.


